Erste Daten der FIRSTANA- und PROSELICA-Studie
Priv.-Doz. Dr. med. Henrik Suttmann
Facharzt für Urologie
Urologikum Hamburg
Harksheider Straße 3
22399 Hamburg
Hintergrund
Im Gefolge der Publikation der TROPIC-Studie wurde Cabazitaxel in der Dosierung 25 mg/qm q3wks als erste Substanz zur Zweitlinientherapie des mCRPC nach Docetaxel in Deutschland zugelassen.1 Hinsichtlich des Stellenwerts von Cabazitaxel in der Sequenztherapie des mCRPC bestehen noch wesentliche offene Fragen, wie z. B. zur Verträglichkeit, optimalen Dosierung sowie Wirksamkeit im Vergleich zu Docetaxel. In Kooperation zwischen der „Food and Drug Administration“ (FDA) und einem Industriesponsor (Sanofi) wurden zwei Phase-III-Studien zur Beantwortung dieser Fragen konzipiert, deren wesentliche Ergebnisse auf dem diesjährigen ASCO-Jahreskongress erstmals vorgestellt wurden.
Studiendesign
FIRSTANA:
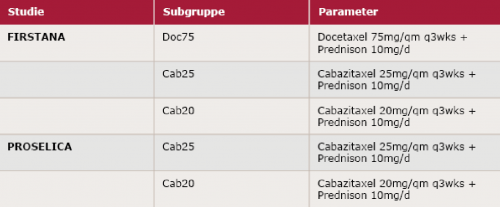
Eine prospektiv-randomisierte dreiarmige Phase-III-Studie an 1.168 Patienten in insgesamt 153 Zentren weltweit mit Chemo-naivem mCRPC zum Vergleich zwischen 1) Docetaxel 75 mg/qm q3wks + Prednison 10 mg/d (P) (Doc75) vs. 2) Cabazitaxel 25 mg/qm q3wks + P (Cab25) vs. 3) Cabazitaxel 20mg/qm q3wks + P (Cab20) (siehe Tab. 1). Als primärer Endpunkt ist das Gesamtüberleben definiert.<2
PROSELICA:
Eine prospektiv randomisierte zweiarmige Phase-III-Studie an 1.200 Patienten in insgesamt 172 Zentren weltweit mit progredientem mCRPC während oder nach vorausgegangener Docetaxel-Chemotherapie zum Vergleich zwischen 1) Cabazitaxel 25 mg/qm q3wks + P (Cab25) vs. 2) Cabazitaxel 20 mg/qm q3wks + P (Cab20) (siehe Tab 1).
Tabelle 1: Einteilung der Studiengruppen der FIRSTANA2 und PROSELICA Studie3
 Ergebnisse
Ergebnisse
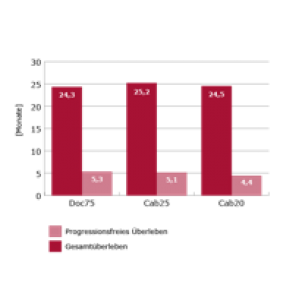
Die Randomisierung in die FIRSTANA-Studie erfolgte zwischen Mai 2011 und April 2013. Die mediane Zyklenzahl in allen drei Behandlungsgruppen betrug 9. Die „intention to treat“(ITT)-Analyse ergab keinen Unterschied bzgl. des Gesamtüberlebens zwischen den Gruppen Doc75, Cab25 und Cab20 – dieses lag bei 24,3 Mon, 25,2 Mon bzw. 24,5 Mon.2
Das progressionsfreie Überleben lag bei 5,3 Mon, 5,1 Mon bzw. 4,4 Mon (Abb. 1).
Abbildung 1: Gesamtüberleben und progressionsfreies Überleben in Studiensubgruppen der FIRSTANA-Studie2

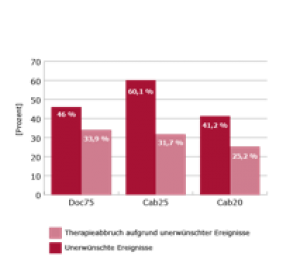
Für Cab25 zeigte sich ein signifikant besseres Tumoransprechen im Vergleich zu Doc75 (41,6 % vs. 30,9 %). Unerwünschte Ereignisse traten unter Doc75 in 46 %, unter Cab25 in 60,1 % und unter Cab20 in 41,2 % der Fälle auf – dies führte in 33,9 %, 31,7 % bzw. 25,2 % der Fälle zum Therapieabbruch (Abb. 2).
Abbildung 2: Unerwünschte Therapieereignisse und daraus folgende Therapieabbrüche in den verschiedenen Subgruppen der FIRSTANA-Studie2
Zusammenfassend traten unter Doc75 vermehrt periphere Polyneuropathien (25,1 % Grad I-IV; 2,1 % Grad III-IV), periphere Ödeme, Alopezien und Nagelveränderungen auf. Demgegenüber waren unter Cab25 febrile Neutropenien (12 %), Durchfälle und Makrohämaturien häufiger.
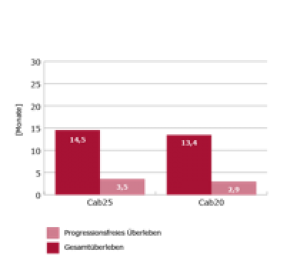
Die Randomisierung in die PROSELICA-Studie erfolgte zwischen April 2011 und Dezember 2013. Die mediane Zyklenzahl betrug für Cab25 = 7 und für Cab20 = 6. In der ITT-Analyse zeigte sich kein Unterschied bzgl. des Gesamtüberlebens zwischen den Gruppen Cab25 und Cab20 – dieses lag bei 14,5 Mon bzw. 13,4 Mon.3Das progressionsfreie Überleben lag bei 3,5 Mon bzw. 2,9 Mon (Abb. 3).
Abbildung 3: Gesamtüberleben und progressionsfreies Überleben in den Subgruppen der PROSELICA-Studie3
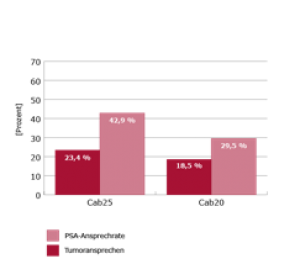
Es zeigte sich ein signifikant besseres Tumoransprechen zugunsten von Cab25 vs. Cab20 (23,4 % vs. 18,5 %) sowie eine signifikant bessere PSA-Ansprechrate (42,9 % vs. 29,5 %) (Abb. 4).
Abbildung 4: Tumoransprechrate und PSA-Ansprechrate in den Subgruppen der PROSELICA-Studie3
Unter Cab25 traten febrile Neutropenien (9,2 %), Durchfälle sowie Hämaturien häufiger auf als unter Cab20.
Bewertung und Diskussion
Docetaxel bleibt in der Dosierung 75 mg/qm q3wks beim mCRPC die Chemotherapie der ersten Wahl. Die Behandlungsrealität beim fortgeschrittenen Prostata-CA hat sich allerdings in den vergangenen Jahren kontinuierlich verändert. So erhalten viele Patienten 6 Zyklen Docetaxel bereits „upfront“ beim metastasierten hormonnaiven Prostata-CA (mHNPC), entweder beim „de novo“-mHNPC oder beim systemischen Progress nach Versagen einer lokalen Therapiemaßnahme. In diesen Fällen wird sich die erneute Frage nach einer geeigneten zweiten Chemotherapie erst nach einer langen, oft mehrjährigen progressionsfreien Zeit unter androgendeprivativer Therapie (ADT) und ggf. nach diversen Interventionen mit 2. Generations-Hormontherapien (Abirateron oder Enzalutamid) stellen. Hier spricht die deutlich bessere Verträglichkeit von Cab20 im Vergleich zu Cab25 bei vergleichbarer klinischer Wirksamkeit nun eher für die reduzierte Dosis.
Zwar zeigten Subgruppenanalysen der PROSELICA-Studie einen Trend zugunsten einer besseren Wirksamkeit von Cab25, insbesondere bei Abirateron- bzw. Enzalutamid-vorbehandelten Patienten.3 So lange jedoch keine detaillierteren Daten zur Folgetherapie aus dieser Studie bekannt sind, lassen sich hieraus keine verlässlichen Schlüsse ableiten.
Auffällig erscheint die große Varianz der bisher publizierten Daten zu den als besonders problematisch diskutierten unerwünschten Ereignissen wie febrile Neutropenien und peripherer Polyneuropathien unter Cab25. So wird die febrile Neutropenierate unter Cab25 mit zwischen 3,3 % in einem „expanded access“-Programm (EAP) und bis zu 12 % in der FIRSTANA-Studie angegeben2,4, wobei wahrscheinlich die im Rahmen einer Phase-III-Studie systematisch erfassten Daten im Vergleich zu einem EAP ohne „monitoring“ die Realität besser widerspiegeln. Unter Cab20 beträgt die febrile Neutropenierate lediglich zwischen 2,1 % (PROSELICA) bis 2,4 % (FIRSTANA).
Interessanterweise ist sie somit sowohl unter Cab25 als auch unter Cab20 in der „first line“-Indikation tendenziell etwas höher als bei den bereits chemotherapeutisch vorbehandelten, mutmaßlich „krankeren“ Patienten in der „second line“.2,3 Periphere Polyneuropathien treten unter Doc75 mit 25,1 % mehr als doppelt so häufig auf wie unter Cab20 und Cab25 (11,7 % bzw. 12,3 %). Des Weiteren finden sich periphere Polyneuropathien der Grade III-IV fast ausschließlich unter Doc75 (2,1 % vs. 0,3 % bzw. 0 %). Somit stellt in der urologischen Praxis Cab20 im Vergleich zu Cab25 bzw. auch zu einer Doc75-„rechallenge“ bei mCRPC-Patienten in Progression nach vorausgegangener Docetaxel-Chemotherapie eine attraktive Alternative dar.
(1) de Bono, J. S. et al. Prednisone plus cabazitaxel or mitoxantrone for metastatic castration-resistant prostate cancer progressing after docetaxel treatment: a randomised open-label trial. The Lancet, Volume 376, Issue 9747, 1147-1154
(2) Sator, A. O. et al. Cabazitaxel vs docetaxel in chemotherapy-naive (CN) patients with metastatic castration-resistant prostate cancer (mCRPC): A three-arm phase III study (FIRSTANA). J Clin Oncol 34, 2016 (suppl; abstr 5006)
(3) de Bono, J. S. et al. Phase III non-inferiority study of cabazitaxel (C) 20 mg/m2 (C20) versus 25 mg/m2 (C25) in patients (pts) with metastatic castration-resistant prostate cancer (mCRPC) previously treated with docetaxel (D). J Clin Oncol 34, 2016 (suppl; abstr 5008)
(4) Heidenreich A., Pfister D. Cabazitaxel in the Management of Metastatic Castration-resistant Prostate Cancer Progressing After Docetaxel-based Chemotherapy. European Oncology & Haematology, 2012;8(1):42–5